code { background-color: transparent }
En función del foco que pone la FDA en la evidencia del mundo real, las organizaciones de medicamentos y dispositivos procuran, cada vez más, incorporar datos generados por los pacientes en las presentaciones regulatorias correspondientes a nuevos productos e indicaciones de tratamiento. Sin embargo, hasta hace poco, no existían tecnologías o metodologías móviles para recopilar, almacenar y presentar datos de este tipo de una forma que cumpliera con la normativa. A fin de cerrar esa brecha, la FDA desarrolló MyStudies, una plataforma con tecnología de código abierto que facilita que las organizaciones farmacéuticas, biológicas y de dispositivos recopilen y presenten datos del mundo real en sus presentaciones regulatorias.
Google Cloud está trabajando para ampliar la plataforma MyStudies de la FDA con funciones de seguridad incorporadas y controles de privacidad configurables, además de la posibilidad de que las organizaciones de investigación detecten y protejan la información que permitiría identificar a una persona. Cuando una organización implementa FDA MyStudies en Google Cloud, se crea una instancia única y lógicamente aislada de la plataforma, a la que solo la organización y sus delegados tienen autorización para ingresar. Estas tecnologías permiten que una organización de investigación defina cuáles de sus investigadores y clínicos pueden acceder a los datos y ayudan a optimizar el uso de esos datos de acuerdo con las instrucciones de los participantes. Explotando Google Cloud como infraestructura subyacente de las implementaciones de FDA MyStudies, las organizaciones tendrán mayor seguridad respecto de la propiedad y la administración de los datos de sus estudios.
Además, Google Cloud está ofreciendo patrocinio para incorporar el estudio de investigación cardiovascular MyHeart Counts de la Universidad Stanford a la plataforma FDA MyStudies, lo que permitiría que este revolucionario estudio clínico virtual comience a incorporar usuarios de dispositivos iOS y Android. Desde su lanzamiento como una de las aplicaciones de investigación de iOS iniciales, MyHeart Counts incorporó a más de 60 000 participantes y generó un conocimiento significativo respecto de la posibilidad de realizar ensayos clínicos a gran escala basados en smartphones.
Habilitar los datos generados por el paciente con MyStudies
La FDA recurre a ensayos clínicos y estudios enviados por los patrocinadores de los estudios para determinar si aprueba, licencia o autoriza la comercialización de un medicamento, un fármaco biológico o un dispositivo en los Estados Unidos. Históricamente, esa información se ha obtenido de manera casi exclusiva mediante ensayos clínicos tradicionales realizados en condiciones estrictamente controladas. Sin embargo, la creciente digitalización de los datos médicos de los pacientes podría ayudar a mejorar la salud con evidencia del mundo real de alta calidad y ensayos clínicos más eficientes.
La FDA advirtió esa oportunidad. Por ejemplo, el Comité de Asesoramiento para la Comunicación con los Pacientes de la FDA ahora ayuda a garantizar que las experiencias de los pacientes se tengan en cuenta en el contexto de las deliberaciones de la Administración en torno a temas complejos relacionados con la regulación de dispositivos médicos. Además, en 2017, el Centro de Dispositivos y Salud Radiológica de la FDA publicó un documento de orientación referido a la generación de evidencia del mundo real para los dispositivos médicos. La FDA también publicó varios borradores de documentos de orientación sobre desarrollo de medicamentos centrado en el paciente, en los que se aborda cómo las partes interesadas pueden recopilar y enviar datos de la experiencia del paciente a fin de contribuir a la toma de decisiones regulatorias. Por último, en 2018, la FDA también lanzó un Marco de Evidencia del Mundo Real, en el que se detallan las iniciativas de la Administración tendientes a evaluar la evidencia del mundo real correspondiente a medicamentos y fármacos biológicos, según dispone la Ley de Curas del Siglo 21.
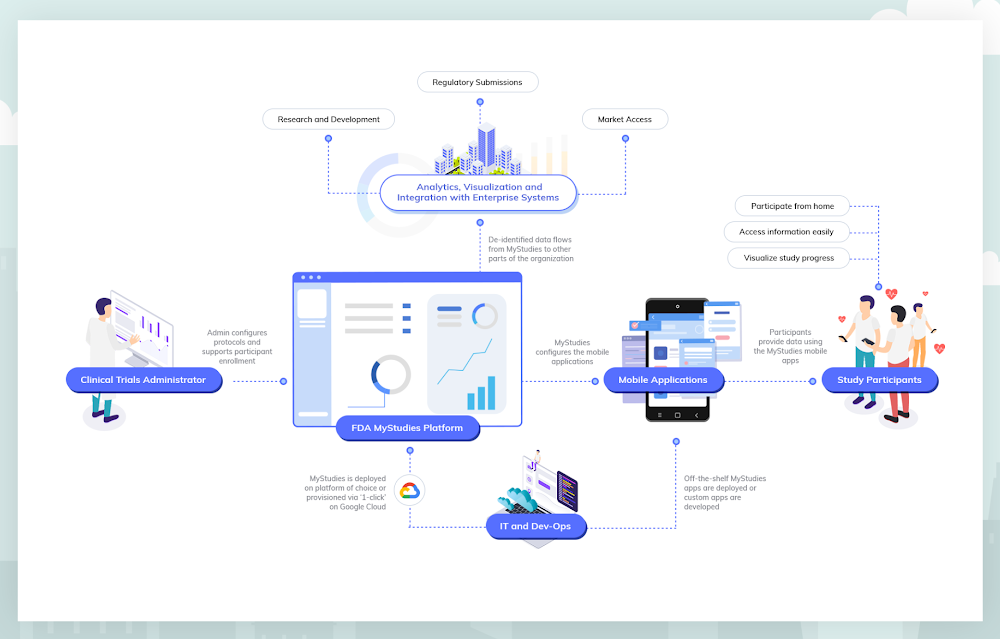
Lanzada originalmente como un recurso disponible de forma pública en noviembre de 2018, la plataforma MyStudies de la FDA incluye funciones importantes que contribuyen a la accesibilidad y la privacidad del paciente. La aplicación para dispositivos móviles de los pacientes se desarrolló con el marco de código abierto ResearchStack para Android y con el marco ResearchKit de Apple para iOS. Mediante estos marcos, los desarrolladores pueden expandir las capacidades de las aplicaciones para dispositivos móviles de código abierto o crear sus propias aplicaciones privadas con marca. Las aplicaciones para dispositivos móviles de MyStudies pueden configurarse para distintas áreas terapéuticas y resultados en términos de salud mediante una interfaz web que reduce la necesidad de desarrollar software personalizado. La plataforma general se diseñó para que sea compatible con los requisitos de auditoría a fin de cumplir con la parte 11 del título 21 del Código de Regulaciones Federales, lo que permite que la plataforma se use para ensayos con supervisión del programa denominado Investigational New Drug (IND).
Los patrocinadores de estudios ya aprovecharon la plataforma MyStudies de la FDA a fin de crear aplicaciones para dispositivos móviles con marca y personalizadas para realizar cuestionarios que evalúan los resultados declarados por los pacientes, los reportes de los pacientes en relación con las recetas y el uso de medicamentos sin receta, los diarios de medicamentos de ensayos clínicos y otros datos relacionados con la experiencia del paciente. Gracias a la incorporación de MyStudies a Google Cloud, a los patrocinadores de nuevos estudios les resultará aún más fácil aprovechar la plataforma.
Nueva plataforma, nuevas oportunidades
Ahora, Google Cloud equipará la plataforma MyStudies de la FDA con un conjunto adicional de capacidades que reducen las complejidades y la sobrecarga, lo que permitirá que las organizaciones farmacéuticas y de tecnología comiencen a trabajar rápidamente. En el caso de los diseñadores de estudios que no deseen configurar desde cero un entorno que cumpla con la normativa, este año se habilitará una opción de «clic para desplegar» en el mercado de Google Cloud. Al usar esa opción para desplegar FDA MyStudies en Google Cloud, se crea una instancia de MyStudies privada a partir del repositorio de código abierto. Esa instancia se configura de acuerdo con las prácticas recomendadas a fin de que funcione con servicios específicos de Google Cloud. Eso permite que los grupos de investigación creen su propia instancia preconfigurada de la plataforma MyStudies de la FDA en cuestión de minutos.
«En función de las obligaciones que asumimos en el contexto de la Ley de Curas del Siglo 21, la FDA emprende proyectos de demostración público-privados a fin de promover la ciencia regulatoria en torno a la evidencia del mundo real. La inversión del Fondo Fiduciario de Investigación de Resultados Centrados en el Paciente que lanzó FDA MyStudies es un paso en esa dirección», dijo el Dr. David Martin, director asociado de Análisis de Evidencia del Mundo Real, Oficina de Política Médica, Centro de Evaluación e Investigación de Medicamentos de la FDA. «FDA MyStudies está disponible de forma pública, pero se necesita experiencia profesional y tiempo para pasar de un recurso de código abierto a la implementación de una plataforma con una nueva marca. Tal como podría hacer una empresa, Google Cloud toma esos recursos para crear una opción de ‘clic para desplegar’ vinculada a la administración y el análisis de datos médicos adicionales».
Además de la implementación optimizada del software de código abierto, las empresas de medicamentos y dispositivos que ejecuten FDA MyStudies en Google Cloud podrán aprovechar la integración con otras ofertas de Google Cloud, por ejemplo, los servicios administrados compatibles con el cumplimiento de HIPAA, como la API de salud y nuestro almacén de datos sin servidores, BigQuery. Aquí puedes obtener más información sobre el cumplimiento en Google Cloud y una lista actualizada de productos cubiertos por nuestro BAA.
Además del cumplimiento de HIPAA, Google Cloud también contribuye al cumplimiento de los clientes de las normativas de la parte 11 del título 21 del Código de Regulaciones Federales si usan Google Cloud de la manera indicada para administrar datos relacionados y cargas de trabajo. Si bien Google tiene una pila de tecnología de nube lista para muchas cargas de trabajo que cumplen con la parte 11 del título 21 del Código de Regulaciones Federales, la definición última respecto del cumplimiento depende de las elecciones del cliente en términos de configuración.
MyHeart Counts + FDA MyStudies en Google Cloud
En 2015, la Universidad Stanford hizo historia en el terreno de la salud en teléfonos celulares cuando lanzó MyHeart Counts en el contexto del primer grupo de aplicaciones de investigación para iOS. Por tratarse de un estudio de inscripción abierta, toda persona que cumpla con los requisitos y descargue MyHeart Counts puede ofrecer su consentimiento para participar de una investigación cardiovascular. Una vez inscritos, los participantes reciben preguntas de encuesta relacionadas con su salud y su nivel de actividad física. Los participantes pueden permitir que MyHeart Counts recopile datos de actividad física de sus teléfonos y otros dispositivos wearable. Si los participantes están en condiciones físicas de hacerlo, se les pide que hagan una caminata de prueba de 6 minutos y que ingresen datos sobre factores de riesgo y análisis de sangre, que se utilizan para determinar un puntaje de riesgo vascular.
La versión actual de MyHeart Counts solo está disponible en dispositivos iOS. Usando FDA MyStudies en Google Cloud, los investigadores de Stanford responsables de MyHeart Counts realizarán un ensayo controlado aleatorio en varios frentes que se ejecutará en dispositivos iOS y Android (el primero de su tipo). Las mejoras adicionales de la plataforma FDA MyStudies permitirán que los investigadores, como aquellos que dirigen MyHeart Counts, configuren y desplieguen estudios en cuestión de días, en lugar de tardar meses, y sin necesidad de desarrollar software.
El estudio se está realizando bajo la supervisión del Prof. Euan Ashley, MBChB, DPhil, profesor de Medicina, de Genética y de Ciencias de Datos Biomédicos en Stanford. «En esta era digital en la que todos usan un smartphone, realizar un ensayo en una app nos permite trabajar con una enorme población. Agradecemos el apoyo de Google, ya que nos permite expandir nuestro alcance para sumar participantes de Android a los de iOS e incorporar un ensayo controlado aleatorio de inscripción abierta en una aplicación para dispositivos móviles por primera vez», dijo el profesor Ashley.
«MyHeart Counts y otras apps digitales de ese tipo permiten que los expertos se conecten directamente con los pacientes de una forma que es más inmediata y más amplia, mediante la recopilación directa de mediciones a partir de sensores. El apoyo que Google Cloud brinda a estas iniciativas no solo ayuda a los investigadores a organizar y a implementar importantes programas de investigación más rápido y de forma más confiable, sino que, en última instancia, ayudará a que los pacientes y sus médicos detecten antes los problemas de salud, lo que les permitirá abordarlos más rápido», dijo el profesor Ashley.
Lo que viene
En pos de nuestro compromiso con la salud y el código abierto, Google Cloud seguirá invirtiendo en MyStudies para incorporar mejoras generales a la plataforma, ampliar la cantidad de evaluaciones compatibles y habilitar la integración con herramientas de análisis y visualización descendentes.
Comunícate para obtener más información y recibir notificaciones respecto del momento en el que MyStudies pasará a estar disponible en el mercado de Google Cloud.
Source: Google Dev